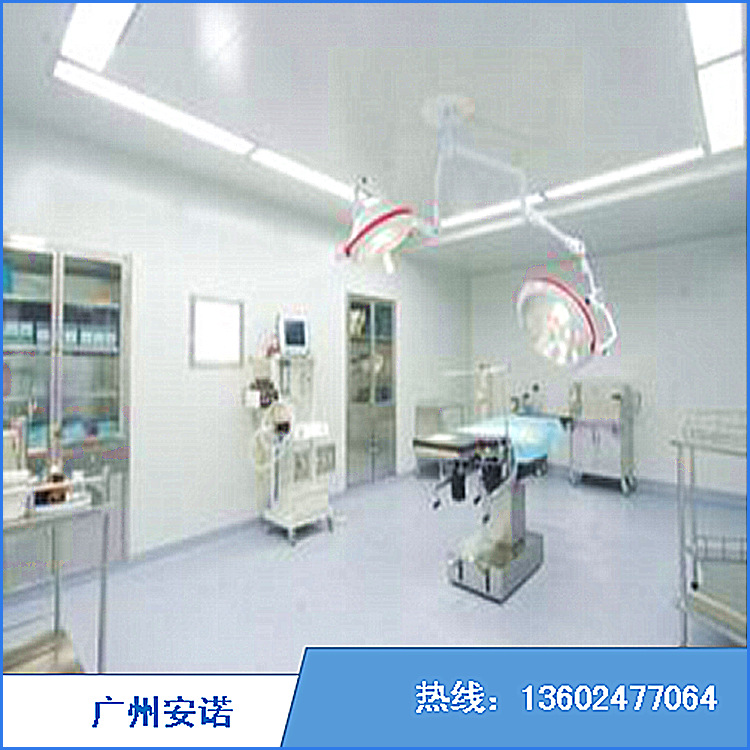
GMP製藥無塵車間特點
1、生物製藥無塵車間不僅設備費用高、生產工藝復雜、潔凈級別和無菌的要求高,而且對生產人員的素質有嚴格的要求。
2、在生產過程中會出現潛在的生物危害,主要有(感染危險,死菌體或死細胞及成分或代謝對人體和其他生物致毒性、致敏性和其他生物學反應,產品的致毒性、致敏性和其他生物學反應,環境效應。)
潔凈區(Clean Area)
需要對環境中塵粒及微生物污染進行控製的房間(區域),其建築結構、裝備及其使用均具有防止該區域內污染物的引入、產生和滯留的功能。
氣鎖間(Air Lock)
設置於兩個或數個房間之間(如不同潔凈度級別的房間之間)的具有兩扇或多扇門的隔離空間。設置氣鎖間的目的是在人員或物料出入其間時,對氣流進行控製。氣鎖間有人員氣鎖間和物料氣鎖間之分。

生物製藥無塵車間的基本特征:是必須以塵粒和微生物為環境控製對象。
生物製藥無塵車間潔凈度共分四個級別:100級或10000級背景下的局部100級、1000級、10000級和30000級。
潔凈室的溫度:在無特殊要求下,在18~26度,相對濕度控製在45%~65%。
生物製藥無塵車間污染控製:污染源控製,散播過程控製,交叉污染控製。
醫藥廠房凈化室關鍵技術主要在於控製塵埃和微生物,作為污染物質,微生物是醫藥廠房凈化室環境控製的重中之重。醫藥廠房潔凈區的設備、管道內積聚的污染物質,可以直接污染藥品,卻毫不影響潔凈度檢測,所以我們說:GMP需要空氣凈化技術,而空氣凈化技術不代表GMP!潔凈度等級不適用於表征懸浮粒子的物理性、化學性、放射性和生命性。不熟悉藥品生產工藝和過程,不瞭解造成污染的原因和污染物質積聚的場所,不掌握清除污染物質的方法和評價標準。
GMP技術改造醫藥廠房工程普遍存在以下情況
正由於存在主觀認識上的誤區,在污染控製過程中的潔凈技術應用不利,最終出現瞭有的藥廠投入巨資改造後,藥品質量並未明顯提高。
醫藥潔凈生產廠房的設計、施工、廠房內設備設施的製造、安裝,生產用原輔物料、包裝材料質量、人凈物凈設施控製程序執行不利等都會影響產品質量。

施工方麵影響產品質量的原因是過程控製環節有問題,在安裝施工過程中留有隱患,有如下具體表現:
①凈化空調系統風道內壁不乾凈、連接不嚴密、漏風率過大;
②彩鋼板圍護結構不嚴密,潔凈室與技術夾層(吊頂)的密封措施不當、密閉門不密閉;
③裝飾型材及工藝管線在潔凈室形成瞭死角、積塵;
④個別位置未按照設計要求施工,無法滿足相關要求規定;
⑤所用密封膠質量不過關、易脫落、變質;
⑥回、排風彩鋼板夾道相通,粉塵從排風到進入回風道;
⑦工藝純化水、註射水等不銹鋼衛生管道焊接時內壁焊縫未成型;
⑧風道止回閥動作失靈,空氣倒灌造成污染;
⑨排水系統安裝質量不過關、管架、附件易積塵;
⑩潔凈室壓差整定不合格,未能滿足生產工藝要求。


批發市場僅提供代購諮詢服務,商品內容為廠商自行維護,若有發現不實、不合適或不正確內容,再請告知我們,查實即會請廠商修改或立即下架,謝謝。